Las adicciones —ya sea a sustancias (cocaína, alcohol, opioides, nicotina) o conductuales (juego patológico, trastorno por videojuegos)— representan un desafío clínico de primera magnitud. A pesar de los avances en psicofarmacología y terapias psicosociales, las tasas de recaída se mantienen alarmantemente elevadas: se estima que hasta el 90% de los individuos recaen dentro de los 6 meses posteriores al inicio del tratamiento. Esta realidad ha impulsado la búsqueda de intervenciones que actúen directamente sobre los circuitos cerebrales desregulados. Entre ellas, la Estimulación Magnética Transcraneal (EMT) se perfila como una herramienta prometedora, no invasiva y con un perfil de seguridad favorable.
2. Fundamentos neurobiológicos aplicados a la adicción
Desde la neurociencia actual, la adicción se entiende como un trastorno de la neuroplasticidad. Tres sistemas son clave:
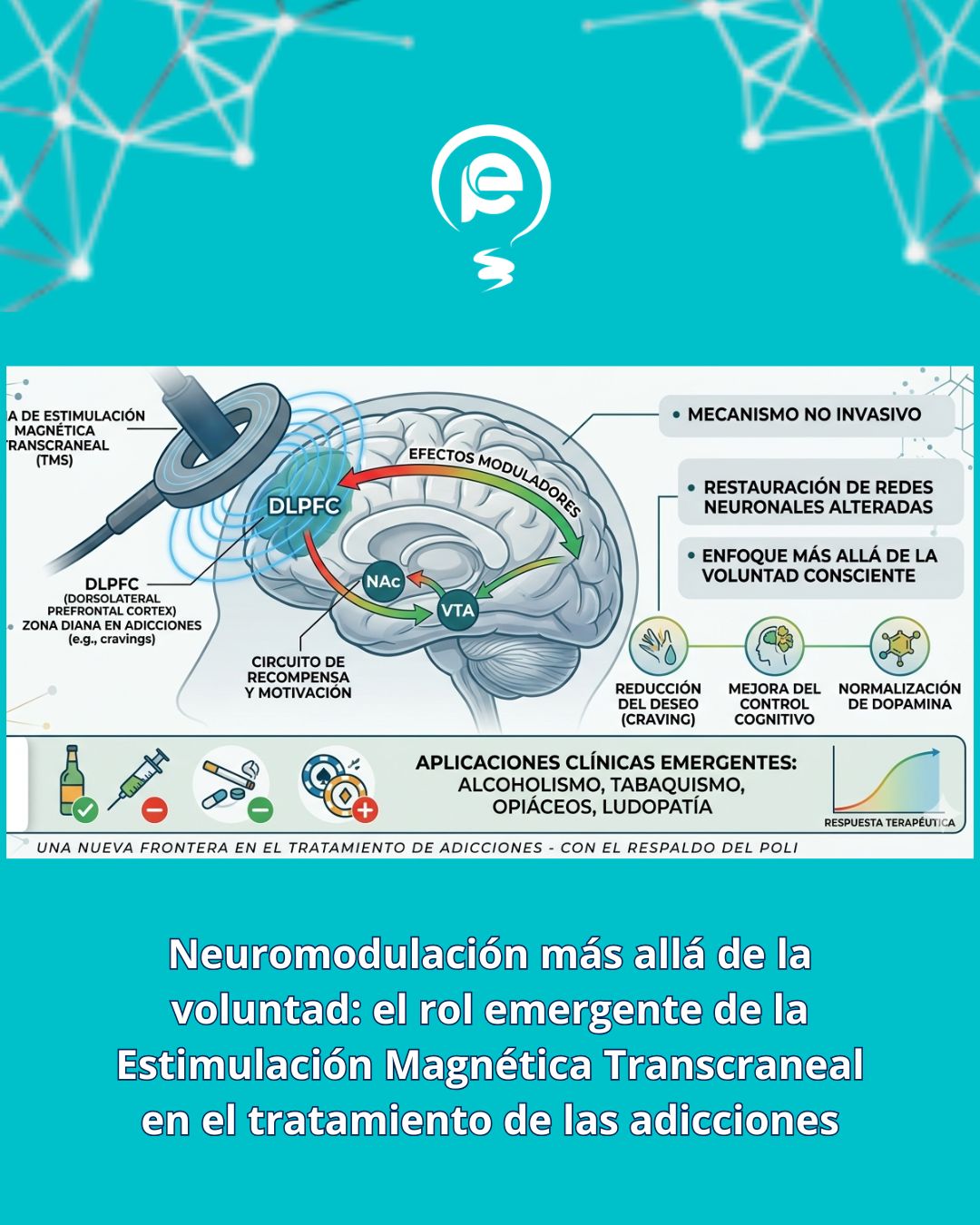
– Corteza prefrontal dorsolateral (CPFDL): Responsable del control ejecutivo y la toma de decisiones. En adicción crónica, muestra hipoactividad metabólica generalizada, lo que se traduce en una capacidad deteriorada para inhibir el craving.
– Corteza cingulada anterior y núcleo accumbens: Implicados en la saliencia del incentivo y la búsqueda compulsiva de la droga.
– Ínsula y amígdala: Procesan el craving o deseo intenso, desencadenante central de la recaída.
La EMT permite modular la excitabilidad cortical en regiones específicas. La evidencia neurofisiológica indica que la estimulación de alta frecuencia (>5 Hz) induce cambios similares a la potenciación a largo plazo (LTP), mientras que la baja frecuencia (≤1 Hz) produce efectos inhibitorios análogos a la depresión a largo plazo (LTD) .
3. Mecanismos de acción y resultados clínicos
La EMT repetitiva (EMTr) aplicada a altas frecuencias sobre la CPFDL izquierda aumenta la liberación de dopamina en el estriado y restaura el equilibrio entre el sistema impulsivo y el sistema reflexivo.
3.1 Efectos sobre el craving: persistencia temporal y papel del placebo
Un estudio observacional de casos y controles con 42 individuos con trastorno por juego de apuestas o consumo de cocaína demostró que, aunque inicialmente los grupos real y placebo mostraban tendencias similares, el grupo de EMTr real presentó una disminución lineal prolongada del craving que se mantuvo hasta 24 semanas (p<0.001). En contraste, el grupo placebo retornó a los niveles iniciales aproximadamente a las 12 semanas (tendencia cuadrática, p<0.001). Este hallazgo sugiere que la EMT real induce cambios neuroplásticos duraderos, mientras que el efecto placebo es transitorio.
3.2 Evidencia cuantitativa por tipo de adicción
Tabaquismo: Un metaanálisis de 17 ensayos controlados aleatorizados (ECA) con 859 participantes reveló que la EMTr reduce significativamente el craving medido por el Cuestionario de Urgencia por Tabaquismo (Diferencia de Medias = -10.89; IC95%: -12.94 a -8.85; p<0.00001). Además, la tasa de abstinencia autoinformada mejoró significativamente (Riesgo Relativo = 1.89; IC95%: 1.12 a 3.19; p=0.02) .
Estimulantes y adicciones conductuales: Un metaanálisis previo que incluyó 34 estudios (42 unidades de análisis) demostró un tamaño del efecto pequeño pero significativo a favor de la EMTr activa sobre placebo en la reducción del craving, siendo este efecto persistente únicamente para los grupos de adicción a estimulantes (nicotina, cocaína, metanfetamina) y conductuales (juego, trastornos alimentarios). No se encontraron diferencias significativas entre diferentes combinaciones de diana y frecuencia de estimulación, pero sí una correlación significativa entre el número de sesiones y la magnitud de la reducción del craving.
Alcohol: Un ensayo controlado aleatorizado en curso con estimulación profunda (dTMS) plantea la hipótesis de que protocolos de estimulación theta-burst intermitente (iTBS) sobre la CPFDL pueden recalibrar la conectividad reducida en esta vía, mientras que la estimulación continua (cTBS) sobre la corteza prefrontal ventromedial (CPFVM) podría atenuar la hiperactividad de la vía de recompensa.
4. Seguridad: Datos de 4,299 participantes
Una revisión sistemática que incluyó 141 ensayos clínicos controlados con 4,299 participantes con trastornos por consumo de sustancias (TCS) evaluó la seguridad de la EMTr en diferentes estadios de la adicción (consumo activo, pretratamiento, recuperación temprana o sostenida). Los resultados fueron concluyentes:
– Sin eventos adversos graves atribuibles: No se reportó ninguna crisis epiléptica inducida por EMTr activa en toda la muestra.
– Perfil de tolerabilidad favorable: El 48.94% de los estudios reportaron únicamente eventos adversos leves y transitorios (cefalea, molestias en el sitio de estimulación, mareo). Solo 9 estudios (6.38%) reportaron abandonos debido a efectos adversos.
Un metaanálisis complementario con 2,865 participantes con TCS cuantificó la prevalencia de efectos secundarios, comparando EMTr activa versus placebo. La prevalencia de efectos graves (crisis epiléptica, sobredosis) no difirió entre grupos. Es relevante que la prevalencia de dolor de cuello y deterioro cognitivo fue mayor en el grupo placebo que en el activo (p<0.05), lo que sugiere que estos síntomas podrían estar relacionados con la expectativa o el procedimiento en sí, no con la neuromodulación activa.
5. Limitaciones actuales y retos metodológicos
– Heterogeneidad de protocolos: No hay consenso sobre el número de sesiones, intensidad, frecuencia o localización precisa. El metaanálisis más amplio hasta la fecha destaca que el 24.82% de los estudios no reportan adecuadamente los eventos adversos, lo que dificulta la estandarización.
– Efecto placebo: Aunque el efecto real es duradero, el placebo tiene un impacto significativo a corto plazo, especialmente en individuos con alta sintomatología psicopatológica.
– Respuesta parcial: Alrededor del 30-40% de los pacientes no responden adecuadamente, lo que subraya la necesidad de biomarcadores predictivos.
6. Perspectivas futuras y estrategias emergentes
– Provocación de síntomas: Un metaanálisis reciente en JAMA Psychiatry sugiere que inducir craving inmediatamente antes de la EMT (por ejemplo, oler un cigarrillo o tocar la suciedad en TOC) podría duplicar la efectividad del tratamiento, aunque se necesitan más ECA para confirmarlo.
– EMT guiada por fMRI: El uso de neuronavegación para dirigir la bobina a la diana óptima de cada paciente (conectividad prefrontal-estriatal) promete aumentar la precisión terapéutica.
– Doble diagnóstico: La EMT está mostrando resultados preliminares prometedores en pacientes con doble diagnóstico (TCS + trastorno psiquiátrico), abordando circuitos neurobiológicos compartidos.
7. Conclusión
La Estimulación Magnética Transcraneal es una intervención segura y bien tolerada para el tratamiento de las adicciones, con evidencia de nivel I que respalda su eficacia en la reducción del *craving* y la prevención de recaídas, particularmente en tabaquismo, cocaína y adicciones conductuales. Los datos de más de 4,000 participantes confirman la ausencia de crisis epilépticas inducidas y un perfil de efectos adversos comparable al de la población general . El futuro pasa por protocolos estandarizados, el uso de provocación de síntomas para aumentar la plasticidad y la integración de la EMT en planes de tratamiento multidisciplinarios.
Referencias clave
1. Souki, A., et al. (2025). Repetitive Transcranial Magnetic Stimulation in Substance Use Disorders is Safe and Tolerable: A Systematic Review of 141 Clinical Trials Including 4,299 Participants. medRxiv.
2. Casula, E. P., et al. (2025). Trend-analysis reveals real and placebo rTMS effects on addiction craving: a case-control observational study. Frontiers in Psychiatry, 15, 1441815.
3. Evidence for safety and tolerability of transcranial magnetic stimulation for substance use disorders. (2025). Brain Stimulation, 18(6), 2043-2049.
4. Efficacy of repetitive transcranial magnetic stimulation for smoking cessation: a systematic review and meta-analysis. (2025). Middle East Current Psychiatry, 32(1).
5. Repetitive Transcranial Magnetic Stimulation (rTMS) as a Promising Treatment for Craving in Stimulant Drugs and Behavioral Addiction: A Meta-Analysis. (2022). Journal of Clinical Medicine, 11(3), 624.
6. Bello, D., et al. (2025). Symptom provocation and clinical response to transcranial magnetic stimulation: a systematic review and meta-analysis. JAMA Psychiatry. doi: 10.1001/jamapsychiatry.2025.0792.


Deja una respuesta